Analisis Keadaan Kimia oleh Spektroskopi Pancaran X-ray Lembut
BERITA JEOL Jld.53 No.5
Masami Terauchi dan Yohei Sato
Pusat Mikroskopi dan Spektroskopi Lanjutan, Institut Penyelidikan Pelbagai Disiplin untuk Bahan Lanjutan, Universiti Tohoku
Pengmetaan Si-sp3 rangkaian Na8Si46 dan taburan keadaan kimia dalam CaB terdop Na6, telah diperhatikan dengan menggunakan instrumen EPMA-SXES komersial. Maklumat yang diperhatikan dalam pelepasan-L bagi 3d unsur logam peralihan yang diperolehi oleh alat SEM-SXES asal dibincangkan.
Pengenalan
Untuk membangunkan bahan berskala nano yang berfungsi dan peranti berskala nano, analisis mikroskopik dan maklum balasnya kepada proses pembuatan adalah isu utama bagi perkembangan tersebut. Untuk tujuan itu, kaedah analisis berdasarkan mikroskop elektron adalah penting. Terutamanya, kaedah spektroskopi memberi kita maklumat berguna yang berkaitan dengan fungsi bahan. Spektroskopi sinar-X untuk analisis unsur mungkin yang paling banyak digunakan. Terdapat dua jenis spektroskopi penyebaran tenaga (EDS) dan spektroskopi penyebaran panjang gelombang (WDS). Spektroskopi kehilangan tenaga elektron (EELS) dan cathodoluminescence (CL, berkaitan dengan peralihan a dalam Rajah 1) juga digunakan secara meluas. Baru-baru ini, wajah baharu spektroskopi pelepasan sinar-X lembut (SXES), yang boleh memberikan maklumat struktur elektronik, masuk ke dalam kumpulan kaedah komersil [1, 2].
Untuk menyiasat struktur elektronik yang berkaitan dengan fungsi bahan, EELS berdasarkan mikroskop elektron penghantaran (TEM) digunakan secara meluas kerana resolusi tenaga yang lebih baik daripada EDS dan WDS dan julat tenaga yang luas 1-1000 eV. EELS boleh memeriksa sifat dielektrik daripada spektrum pengujaan elektron valens (pengujaan b dalam Rajah 1). Terutamanya, pengkomersilan instrumen monokromator baru-baru ini merealisasikan satu probe nanometer dengan resolusi tenaga 0.1 eV atau lebih baik. Ia membolehkan kami menganalisis sifat inframerah hampir bagi zarah nano industri [3] dan juga getaran kekisi haba [4]. Analisis spektrum pengujaan cangkang dalam (pengujaan c dalam Rajah 1) digabungkan dengan simulasi teori menjadi biasa untuk menilai hubungan antara struktur elektronik dan struktur kristal tempatan. Walaupun EELS memberikan banyak maklumat tentang struktur elektronik dari kawasan spesimen berskala nm, ia tidak dapat memberikan maklumat elektron ikatan (jalur valens). Ia boleh direalisasikan oleh SXES, yang menganalisis tenaga pelepasan sinar-X peralihan elektronik d dalam Rajah 1 dengan resolusi tenaga lebih baik daripada 1 eV. Instrumen SXES untuk mikroskop elektron telah dibangunkan untuk TEM [5]. Oleh kerana kecekapan pengesanan yang rendah bagi kaedah tersebut, ia telah dikomersialkan sebagai instrumen untuk penganalisis mikro probe elektron (EPMA) dan mikroskop elektron pengimbasan (SEM) yang boleh menggunakan arus probe yang lebih besar daripada TEM. Memandangkan pelepasan sinar-X untuk analisis unsur (EDS, WDS) secara dominan disebabkan oleh peralihan elektronik antara paras cangkang dalam (peralihan e dalam Rajah 1), spektrum tersebut tidak termasuk maklumat tentang elektron valens.
Rajah 1
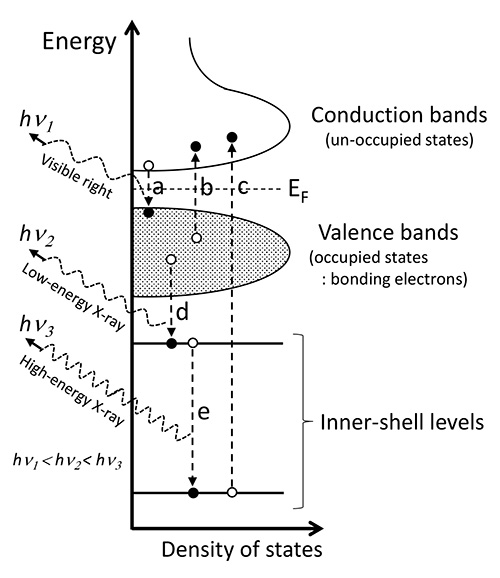
Gambarajah skematik peralihan elektronik yang berkaitan dengan cathodoluminescence (a), pengujaan elektron valens EELS (b), spektrum pengujaan kulit dalam EELS (c), pelepasan sinar-X termasuk maklumat elektron valens (d) dan pelepasan sinar-X yang digunakan terutamanya untuk analisis unsur (e).
Instrumen SXES mula-mula dibangunkan untuk TEM [6]. Leher botol utama untuk aplikasi adalah kecekapan pengesanan yang rendah. Dalam analisis resolusi ruang tinggi spesimen nipis oleh TEM, isipadu spesimen yang diperiksa adalah kecil dan masa pemerolehan beberapa puluh minit atau lebih diperlukan untuk mendapatkan nisbah isyarat kepada bunyi yang munasabah. Apabila menggunakan kaedah ini pada EPMA dan SEM, masa pemerolehan selama satu atau beberapa minit adalah biasa disebabkan oleh arus rasuk yang lebih besar dan volum peperiksaan yang lebih besar. Kaedah SXES ini mungkin berguna sebagai kaedah spektroskopi untuk bahan pukal sebagai kaedah TEM-EELS untuk spesimen nipis. Kemudian, EPMA/SEM-SXES ini boleh membuat maklum balas pantas kepada pemprosesan bahan.
Apabila menggabungkan spektrum EELS pengujaan cangkerang dalam (keadaan kosong yang menyiasat) dan spektrum pancaran sinar-X lembut (keadaan diduduki menyelidik), keadaan elektronik keseluruhan boleh dikira. Tambahan pula, spektrum pengujaan elektronik boleh diperolehi daripada spektrum pengujaan elektron valens EELS dengan menggunakan analisis Kramers-Kronig. Oleh itu, mikroskop elektron boleh menganalisis bukan sahaja struktur kristal dan unsur konstituen tetapi juga struktur elektronik keseluruhan kawasan spesimen kecil yang dikenal pasti [5, 7].
Dalam manuskrip ini, pemerhatian SXES pada pengetatan Si-sp3 rangkaian Na8Si46, taburan keadaan kimia dalam CaB terdop Na6, dan maklumat tentang pelepasan L bagi 3d unsur logam peralihan diterangkan.
Instrumen dan keadaan eksperimen
Instrumen SXES yang digunakan dalam laporan ini ditunjukkan dalam Rajah 2(a) EPMA (JEOL JXA-8230) yang dilampirkan dengan sistem spektrometer SXES komersial (SS-94000SXES) dan (b) SEM (JEOL JSM-6480LV) yang dilampirkan dengan spektrometer asal kami . Kedua-dua instrumen SXES ialah spektrometer jenis WDS berdasarkan optik kejadian ragut medan rata dengan menggunakan jeriji diperbetulkan penyimpangan.
Instrumen SXES komersial dengan dua grating boleh mengesan dari 50 eV hingga 210 eV untuk 1st spektrum pesanan, sehingga 420 eV untuk 2nd spektrum pesanan, dan lebih jauh lagi untuk spektrum pesanan lebih tinggi. Sebenarnya, spektrometer ini boleh mengesan isyarat pancaran sinar-X lembut lebih daripada 70 elemen [8]. Data semasa diukur dengan menggunakan parut JS200N dengan purata ketumpatan alur 1200 garis/mm. Pengesan ialah CCD jenis nipis belakang. Resolusi tenaga yang dinilai untuk struktur tepi Fermi yang tajam diperhatikan untuk pelepasan Al L pada 72 eV ialah kira-kira 0.2 eV. Resolusi tenaga yang tinggi ini membolehkan kami menjalankan pemetaan keadaan ikatan kimia.
Spektrometer SXES asal Rajah 2(b) melakukan julat tenaga yang luas 50-3800 eV untuk spektrum tertib pertama dengan menggunakan empat jeriji. Dalam laporan ini, parut JS1 dengan purata ketumpatan alur 2000 garis/mm telah digunakan. Pengesan plat berbilang saluran yang digabungkan secara optikal dengan kamera CMOS digunakan sebagai pengesan. Instrumen ini melakukan resolusi tenaga 2400 eV dalam mod pengiraan foton untuk pelepasan Al L [0.08].
Pengukuran SXES dilakukan pada voltan pecutan 5 kV. Rajah 2(c) menunjukkan spektrum pancaran Al L, yang menghasilkan peralihan elektronik daripada jalur valens ke paras cengkerang L dalam, yang diperolehi oleh spektrometer komersial. Spektrum menunjukkan struktur tepi Fermi yang tajam pada 72 eV dijangka untuk aluminium, walaupun permukaan spesimen teroksida. Struktur halus akibat pembelahan orbit putaran L3 dan L2 tahap 0.4 eV jelas dilihat. Elektron 5 keV yang dilanggar pada permukaan aluminium tersebar di dalam bahan melalui penyerakan tidak anjal kira-kira 0.32 μm diameter, yang dinilai oleh persamaan Reed d = 0.077 (Eo1.5 - Ec1.5)/ρ (d : saiz penyebaran (μm), Eo : tenaga kejadian (keV), Ec : tenaga pengujaan kritikal untuk sinar-X (keV) yang dikehendaki, ρ: ketumpatan jisim bahan (g/cm3)) [10]. Oleh kerana ketebalan lapisan teroksida permukaan adalah kurang daripada 10 nm, spektrum Rajah 2(c) ditetapkan secara munasabah kepada aluminium tulen. Keamatan pelepasan lapisan teroksida permukaan menjadi jelas untuk voltan pecutan yang lebih rendah daripada 1 kV. Rajah 2(d) menunjukkan spektrum pelepasan Fe L yang diperolehi oleh spektrometer asal kami (Rajah 2(b)) pada voltan pecutan 2, 5 dan 10 kV. Keamatan spektrum telah dinormalkan oleh keamatan pelepasan Lℓ, yang mengalami sedikit kesan penyerapan. Nampaknya dilihat bahawa taburan keamatan pelepasan Lα,β bergantung kepada voltan pecutan. Untuk voltan pecutan yang lebih tinggi, elektron kejadian mencapai kawasan yang lebih dalam dari permukaan spesimen dan menjana pelepasan sinar-X, yang mengalami penyerapan yang lebih besar sebelum keluar dari permukaan. Di rantau tenaga pelepasan-Fe Fe, terdapat kelebihan serapan L pada 707 eV (garis putus-putus merah) antara pelepasan Lα dan Lβ. Ini adalah punca penurunan intensiti Lβ yang banyak untuk voltan pecutan yang lebih besar. Kesan penyerapan adalah lebih kecil untuk voltan pecutan yang lebih rendah, tetapi kesan lapisan teroksida permukaan menjadi jelas. Dengan menggunakan persamaan Reed, sebaran rasuk elektron dalam Fe pada voltan pecutan 15 kV, 5 kV dan 2 kV dinilai masing-masing 0.56 μm, 0.10 μm dan 0.02 μm. Berdasarkan keputusan dan pengalaman eksperimen di atas, voltan pecutan 5 kV telah diterima pakai sebagai keadaan eksperimen yang tidak sensitif permukaan dan kurang kesan penyerapan. Kaedah spektroskopi pada voltan pecutan rendah berguna untuk bahan yang mudah rosak. Baru-baru ini, filem karbon nitrida amorf telah berjaya dianalisis dengan menggunakan SXES pada 5 kV [11].
Rajah 2
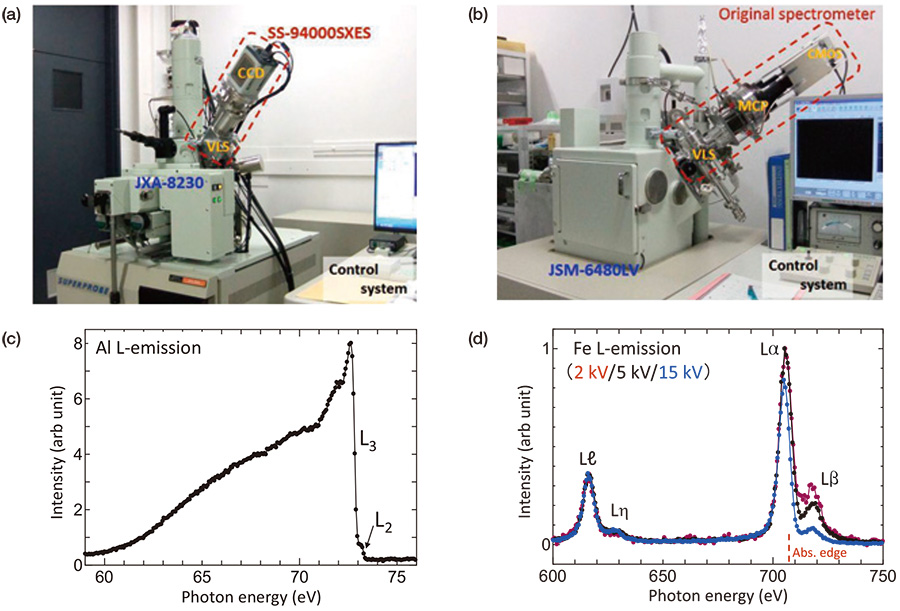
Instrumen SXES yang digunakan dalam laporan ini. (a) EPMA (JEOL JXA-8230) dilampirkan dengan sistem spektrometer SXES komersial (SS-94000SXES) dan (b) SEM (JEOL JSM-6480LV) dipasang dengan spektrometer asal kami. (c) Spektrum pancaran Al-L diperolehi oleh (a). Struktur halus akibat pembelahan orbit putaran L3 dan L2 tahap 0.4 eV dilihat. (d) Spektrum pelepasan Fe L diperolehi oleh spektrometer asal kami (b) pada voltan pecutan 2, 5 dan 10 kV. Keamatan spektrum telah dinormalisasi oleh pelepasan Lℓ.
Metalisasi Si sp3 rangkaian dalam Na8Si46
Rajah 3(a) menunjukkan struktur hablur Jenis-I Na-Si klatrat Na8Si46. Bahan ini berasaskan tiga dimensi Si-sp3 rangkaian ikatan kovalen, yang sepadan dengan penggantian ikatan hidrogen dalam hidrat gas dengan ikatan kovalen Si-Si. Si-sp3 rangkaian ikatan termasuk Si20 (dodecahedron) dan Si24 (tetra-kaidecahedron) sangkar. Atom Na terdapat dalam sangkar tersebut. Si-sp3 rangkaian ikatan mempunyai watak semikonduktor. Walau bagaimanapun, atom Na dalam sangkar memindahkan elektron valensnya ke rangkaian Si menghasilkan watak logam Na8Si46 [12]. Rajah 3(b) menunjukkan imej SEM bagi hablur pukal yang digunakan. Spektrum pelepasan-L Si diperoleh daripada kawasan bulatan di (b) dengan menggunakan instrumen Rajah 2(a) ditunjukkan dalam (c). Spektrum pelepasan Si L bagi wafer Si (semikonduktor) juga ditunjukkan untuk perbandingan. Taburan intensiti tersebut adalah disebabkan oleh peralihan daripada jalur valens kepada Si-L dalaman2,3 tahap dengan p simetri. Disebabkan oleh peraturan pemilihan dipol, taburan keamatan tersebut mencerminkan ketumpatan keadaan jalur valens dengan s and d simetri. Label L2 ' dan L1 yang ditulis dalam spektrum wafer Si menunjukkan titik khas dalam rajah jalur bagi hablur Si kubik. Dua struktur puncak ini nampaknya biasa untuk kedua-dua bahan. Ia mungkin berasal dari Si-sp3 rangkaian ikatan untuk kedua-dua bahan. Bertentangan dengan persamaan ini, hujung sebelah kanan, yang sepadan dengan bahagian atas jalur valens, adalah berbeza antara satu sama lain. Na8Si46 menunjukkan puncak yang tajam. Daripada perbandingan dengan pengiraan teori, puncak tajam ini mungkin ditetapkan kepada keadaan ikatan antara sangkar Si dan atom Na [13]. Untuk menjelaskan perbezaan dengan lebih jelas, spektrum Na8Si46 diperbesarkan dalam Rajah 3(d). Di hujung sebelah kanan spektrum, penurunan intensiti mendadak dengan lebar 0.2-0.3 eV dilihat seperti ditunjukkan oleh garis menegak. Oleh kerana lebarnya adalah setanding dengan resolusi tenaga pengukuran, perubahan keamatan tajam ini boleh diberikan kepada struktur pinggir Fermi, yang nampaknya menunjukkan bahan ini adalah logam.
Rajah 3
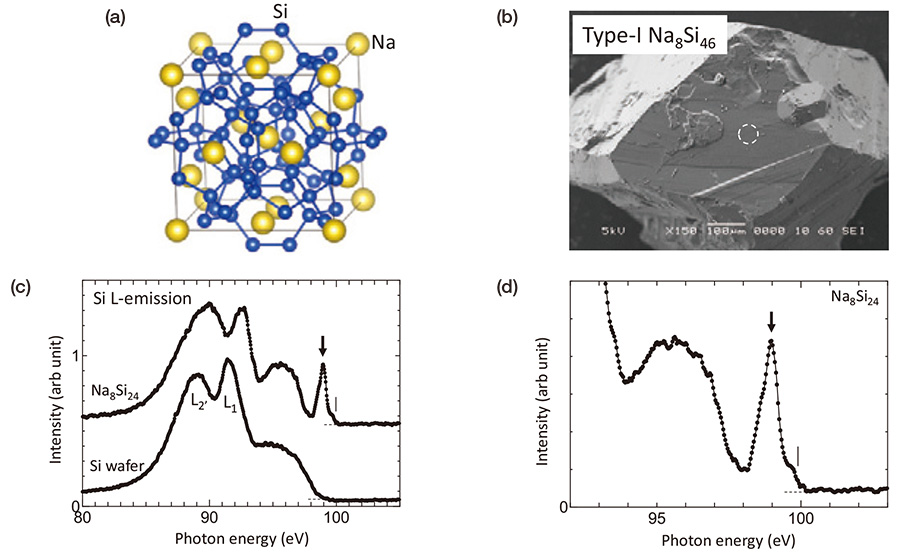
(a) Struktur kristal jenis-I Na-Si klatrat Na8Si46. (b) Imej SEM bagi kristal pukal yang digunakan. (c) Spektrum pelepasan Si L diperolehi daripada kawasan bulatan di (b). (d) Spektrum pembesaran Na8Si46 sepadan dengan bahagian atas jalur valens. Penurunan intensiti mendadak dengan lebar 0.2-0.3 eV, ditunjukkan oleh garis menegak, sepadan dengan struktur tepi Fermi.
Pemetaan keadaan kimia CaB berdop Na6
Struktur kristal CaB6 terdiri daripada rangkaian B6 kelompok oktagon, yang terletak di setiap sudut sel unit padu, dan atom logam pada kedudukan pusat badan sel (Rajah 4(a)). Atom Ca boleh memindahkan dua elektron valens ke B6 rangkaian kluster. Sejak B6 rangkaian kluster boleh menerima dua elektron dalam jalur valens, CaB6 menjadi semikonduktor (n-jenis). Untuk merealisasikan peranti termo-elektrik menggunakan B6 bahan rangkaian kelompok [14], p-jenis semikonduktor adalah perlu. Oleh kerana atom Na mempunyai hanya satu elektron valens, penggantian Na ke tapak Ca ialah doping lubang kepada B6 rangkaian kluster menyebabkan a p-jenis semikonduktor [15]. Daripada penilaian EDS, kandungan Na bahan adalah beberapa peratus. Walau bagaimanapun, keseragaman bahan belum dinilai. Kemudian, sekeping Na-doped CaB6 bahan telah diperiksa dengan menggunakan instrumen SXES-EPMA komersial Rajah 2(a).
Rajah 4(b) dan (c) menunjukkan imej elektron sekunder (SE) dan imej elektron berserakan belakang (BSE) bagi kawasan CaB terdop Na.6, masing-masing. Imej SE menunjukkan sedikit morfologi permukaan yang berbeza di kawasan kiri atas, di mana isyarat karbon dikesan. Imej BSE menunjukkan kawasan keamatan yang lebih rendah di tengah. Kemudian, pengukuran pemetaan SXES telah dijalankan. Peta keamatan spektrum Ca-ℓ, keamatan η (150-154 eV), keamatan BK (170-188 eV), dan bahagian atas keamatan BK (187-188 eV) ditunjukkan dalam Rajah 4(d), (e) dan (f), masing-masing. Peta pelepasan Ca-ℓ, η menunjukkan keamatan rendah untuk kawasan gelap imej BSE. Ia bermakna kandungan Ca yang rendah untuk kawasan tersebut. Peta pelepasan BK tidak menunjukkan perubahan intensiti yang jelas untuk kawasan tersebut. Sebaliknya, peta bahagian atas keamatan pelepasan BK dalam Rajah 4(f) menunjukkan keamatan yang lebih besar untuk kawasan tersebut. Untuk menyiasat asal-usul peningkatan keamatan ini, spektrum pelepasan BK bagi titik A dan B yang ditunjukkan dalam rajah ditunjukkan dalam Rajah 5. Spektrum menunjukkan sedikit perbezaan dalam taburan keamatan tersebut, mencadangkan beberapa perbezaan keadaan ikatan B6- rangkaian kluster. Perlu diperhatikan bahawa puncak spektrum A yang ditunjukkan oleh anak panah terletak di bahagian tenaga yang lebih tinggi sebanyak kira-kira 0.7 eV berbanding dengan spektrum B. Anjakan spektrum A ini sepatutnya merupakan anjakan kimia yang berasal daripada anjakan tenaga pada aras B 1s. kepada bahagian tenaga pengikat yang lebih besar. Peralihan tahap teras ini boleh disebabkan oleh penurunan cas valens atom B. Ia dijangka untuk CaB berdop Na6. Malangnya, sistem sekarang tidak dapat mengesan keamatan pelepasan Na-K (akan muncul tidak lama lagi sebagai versi komersial). Oksigen kekotoran juga boleh menjadi asal kerana atom O menerima elektron. Sebenarnya, keamatan kecil pada 175 eV dalam spektrum A boleh diberikan kepada 3rd perintah intensiti pelepasan OK. Bagaimanapun, pemetaan sinar-X lembut resolusi tenaga tinggi boleh memberi kita pemetaan anjakan kimia yang mencerminkan jumlah cas valens.
Rajah 4
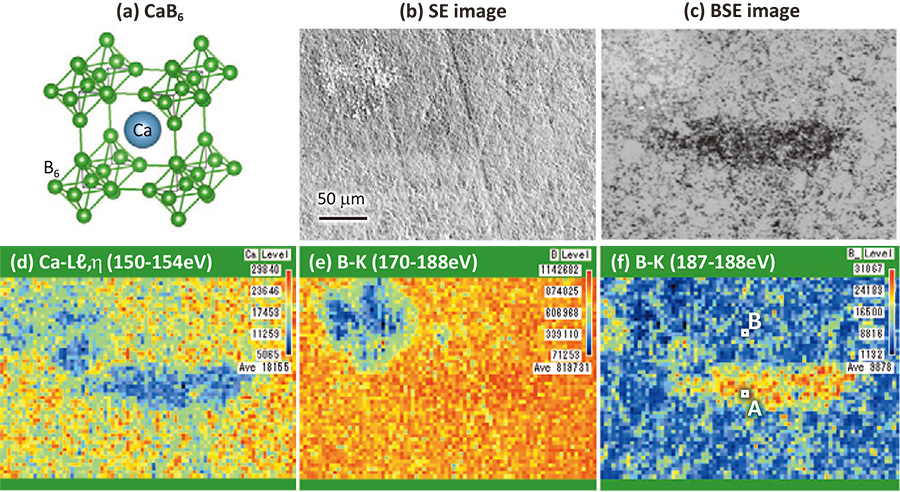
(a) Struktur kristal CaB6. (b) Imej elektron sekunder (SE) dan (c) imej elektron berselerak belakang (BSE) bagi CaB terdop Na6. Peta keamatan spektrum (d) Ca-ℓ, keamatan η (150-154 eV), (e) keamatan BK (170-188 eV), dan (f) bahagian atas keamatan BK (187-188 eV).
Rajah 5
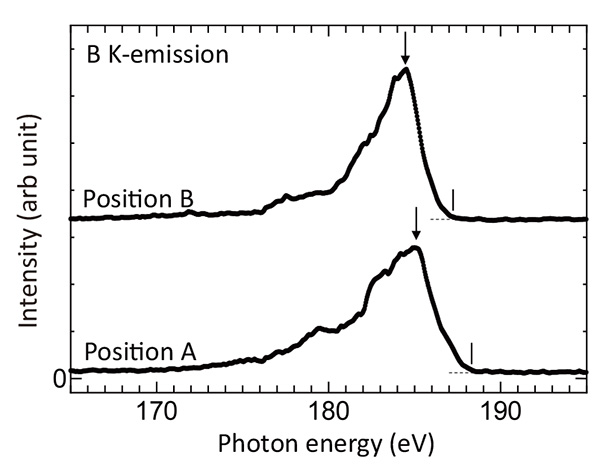
Spektrum pelepasan BK bagi titik A dan B ditunjukkan dalam Rajah 4(f).
Maklumat tentang pelepasan L 3d unsur logam peralihan
Keadaan ikatan dan valensi 3d logam peralihan (3d-TM) adalah kunci untuk menilai bahan elektrod positif bateri Li-ion, kerana perubahan valensi 3d-Elemen TM ialah asal cas dan nyahcas bateri. Maklumat tentang elektron valens 4s dan 3d daripada 3d -Elemen TM termasuk dalam pelepasan L unsur. Sebagai tenaga 1st spektrum tertib berada di luar julat tenaga spektrometer SXES komersial, spektrometer asal (Rajah 2(b)) digunakan untuk menilai spektrum pelepasan-L Ti dan oksidanya [16], dan Fe dan oksidanya. Terdapat empat jenis pelepasan L bagi Lα, Lβ , Lℓ dan Lη . Lα dan Lβ pelepasan adalah disebabkan oleh peralihan elektron valens kepada L dalam3-cangkang dan L2-shell, masing-masing. Oleh itu, keamatan tersebut termasuk maklumat tentang keadaan tenaga 3d elektron. Sebaliknya, Lℓ dan Lη pelepasan adalah disebabkan oleh peralihan dari tahap kulit dalam cetek M1 ke L yang lebih dalam3 dan L2 tahap, masing-masing. Oleh itu, maklumat termasuk dalam Lℓ,η , berbeza dengan Lα,β. Rajah 6 menunjukkan rajah skematik peralihan tersebut. Peralihan dari M2,3 kepada L2,3 dilarang oleh peraturan pemilihan dipol.
Rajah 7 menunjukkan (a) L α,β pelepasan dan (b) Lℓ,η spektrum pelepasan logam-Ti, mono-oksidaε-TiO dan TiO yang dilaporkan baru-baru ini2 (rutil). Jelas dilihat bahawa taburan intensiti pelepasan L α, β adalah berbeza untuk bahan yang berbeza. Ini mencerminkan bahawa keadaan tenaga elektron ikatan adalah berbeza untuk susunan atom atau struktur kristal yang berbeza. Dalam model ionik ringkas, TiO2 dianggap sebagai Ti4+O-22 dan tidak boleh mengeluarkan keamatan L α,β kerana Ti4+ ion tidak mempunyai 3d elektron. Oleh kerana pelepasan L α,β diperhatikan dalam eksperimen, atom Ti dalam TiO2 bukan Ti tulen4+ ion melalui ikatan kovalen antara Ti dan atom O di sekelilingnya. Untuk membincangkan taburan intensiti pelepasan L α, β, bukan sahaja ketumpatan keadaan jalur valens tetapi juga peralihan tenaga paras cengkerang dalam (anjakan kimia) perlu dipertimbangkan. Tambahan pula, pertindihan taburan intensiti Lα dan Lβ dan kehadiran kelebihan penyerapan antara Lα dan Lβ perlu diambil kira. Sebaliknya, taburan intensiti Lℓ,η disebabkan oleh peralihan antara dua tahap cangkerang dalam adalah lebih mudah untuk dibincangkan.
Lα tenaga puncak TiO2 adalah kira-kira 2 eV lebih kecil daripada logam-Ti. Sebaliknya, Lℓ tenaga puncak TiO2 adalah 0.7 eV lebih besar daripada logam-Ti. L kedudukan daripada ε-TiO hampir sama dengan logam-Ti. Dalam kes Fe dan oksidanya ditunjukkan dalam Rajah 7(c), Lℓ logam-Fe dan Fe3O4 ialah kedudukan tenaga yang hampir sama. L daripada Fe2O3 memposisikan bahagian tenaga yang lebih tinggi sedikit iaitu kira-kira 0.2 eV daripada yang lain. Mereka mencadangkan bahawa asal-usul peralihan tenaga Lα dan Lβ tidak mudah. Nisbah keamatan yang lebih besar daripada Lβ /Lα dalam oksida Fe boleh disebabkan oleh penindasan proses Coster-Kronig dalam oksida [18].
Berdasarkan perbincangan tentang anjakan tenaga mengikat akibat perubahan kesan kimia dalam spektroskopi fotoelektron sinar-X, maklumat termasuk dalam Lα dan keamatan pelepasan Lℓ disimpulkan seperti berikut [16]. Perubahan Lα taburan keamatan pelepasan mencerminkan perubahan cas valens dan kesan keadaan pepejal (bidang kristal, ketumpatan keadaan, celah jalur dan sebagainya). Perubahan kedudukan puncak Lℓ disebabkan oleh perubahan M1 kesan lubang teras dalam keadaan akhir, yang mencerminkan kesan saringan tempatan. Kod WIEN2k digunakan untuk menilai perbezaan kesan lubang teras dalam logam dan oksidanya. Nilai TiO2 dibandingkan dengan logam-Ti dan Fe2O3 berbanding dengan logam-Fe ialah +0.7 eV dan +0.2 eV, masing-masing. Nilai tersebut menghasilkan semula nilai yang diperhatikan secara eksperimen. Peralihan puncak ini disebabkan oleh kesan lubang teras berkait rapat dengan sifat dielektrik, tenaga jurang jalur bagi bahan yang diperiksa [19, 20].
Rajah 6
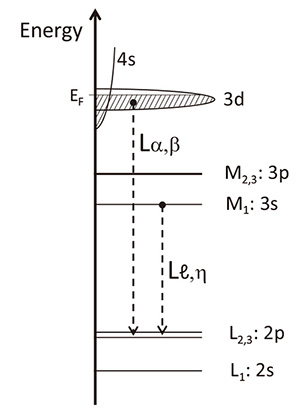
Gambarajah skematik peralihan elektronik yang berkaitan dengan pelepasan Lα,β dan Lℓ,η.
Rajah 7
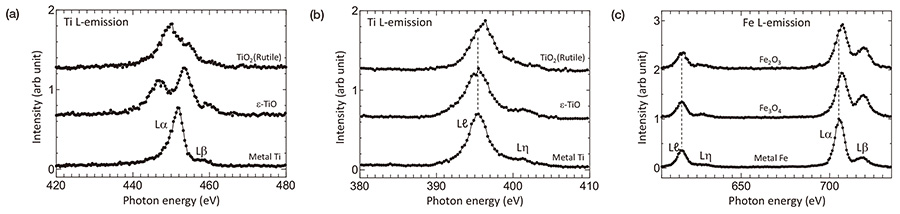
(a) pelepasan Lα,β dan (b) Lℓ,η spektrum pelepasan logam-Ti, ε-TiO dan TiO yang dilaporkan baru-baru ini2 (rutil). (c) Spektrum pelepasan Fe L bagi logam-Fe dan oksidanya.
Kesimpulan
Instrumen SXES yang dikomersialkan baru-baru ini untuk EPMA dan SEM mempunyai resolusi tenaga 0.2 eV untuk pelepasan Al-L, iaitu kira-kira 10-100 kali lebih baik daripada WDS dan EDS. Kaedah SXES ini berguna sebagai kaedah spektroskopi untuk analisis keadaan kimia dan pemetaan bahan pukal sebagai kaedah TEM-EELS untuk spesimen nipis. Oleh kerana tidak memerlukan penyediaan spesimen nipis, EPMA/SEM-SXES ini boleh membuat maklum balas pantas kepada proses pengeluaran bahan. Instrumen ini menyediakan kaedah spektroskopi elektron ikatan bukan sahaja untuk pelbagai jenis perkembangan bahan berfungsi baharu tetapi juga untuk penyelidikan asas sebatian.
Penghargaan
Penulis mengucapkan terima kasih kepada Dr. H. Morito dari Institut Penyelidikan Bahan, Universiti Tohoku kerana membekalkan kristal tunggal klatrat Na-Si. Kajian SXES mengenai CaB berdop Na6 ialah penyelidikan bersama dengan Prof. M. Takeda dari Universiti Teknologi Nagaoka. Penilaian anjakan kimia pelepasan L sebanyak 3d unsur logam peralihan dengan menggunakan kod WIEN2k adalah hasil kerjasama dengan Dr. S. Koshiya dan Dr. K. Kimoto dari Institut Sains Bahan Negara. Kerja-kerja tersebut sebahagiannya disokong oleh Program Penyelidikan "Perikatan Dinamik untuk Inovasi Terbuka Merapatkan Manusia, Alam Sekitar dan Bahan" dalam "Pusat Penyelidikan Bersama Rangkaian untuk Bahan dan Peranti".
Rujukan
- H. Takahashi, T. Murano, M. Takakura, N. Handa, M. Terauchi, M. Koike, T. Kawachi, T. Imazono, N. Hasegawa, M. Koeda, T. Nagano, H. Sasai, Y. Oue, Z. Yonezawa dan S. Kuramoto, Berita JEOL , 49, 73 (2014).
- H. Takahashi, T. Murano, M. Takakura, S. Asahina, M.Terauchi, M. Koike, T. Imazono, M. Koeda dan T. Nagano, IOP Conf. Siri: Sains Bahan dan Kejuruteraan , 109, 012017 (2016).
- Y. Sato, M. Terauchi dan K. Adachi, Jurnal Fizik Gunaan , 112, 074308 (2012).
- OL Krivanek, TC Lovejoy, N. Dellby, T. Aoki, RW Carpenter, P. Rez, E. Soignard, J. Zhu, PE Batson, MJ Lagos, RF Egerton dan PA Crozier, Alam, 514, 209 (2014).
- M. Terauchi, bab 7 dalam Pencirian Mikroskopi Elektron Penghantaran Bahan Nano , ed. Kumar CSSR (Springer-Verlag), 287 (2014).
- M. Terauchi, H. Yamamoto dan M. Tanaka, Jurnal Mikroskopi Elektron , 50, 101 (2001).
- M. Terauchi dan M. Kawana, Ultramikroskopi , 106, 1069 (2006).
- M. Terauchi, H. Takahashi, M. Takakura dan T. Murano, Buku Panduan Spektra Pancaran X-ray Lembut ver. 3 (IMRAM Tohoku Univ. & JEOL), (2016).
- M. Terauchi, H. Takahashi, M. Takakura, T. Murano, M. Koike, T. Imazono, T. Nagano, H. Sasai dan M. Koeda, Mikroskopi dan Mikroanalisis , 22(Bekalan 3), 414 (2016).
- SJB Reed, Analisis Mikroprob Elektron edisi ke-2 (Cambridge Univ. Press.), 200 (1993).
- S. Ishii, M. Terauchi, Y. Sato, N. Tamura, M. Aono dan H. Abe, diserahkan kepada Mikroskopi (2018).
- A. Moewes, EZ Kurumaev, JS Tse, M. Geshi, MJ Ferguson, VA Trofimova dan YM Yarmoshenko, Fizik. Rev. B, 65, 153106 (2002).
- Z. Wei, C. Quing-Yun, Z. Zhao-Yi dan C. Ling-Cang, Dagu. Fizik. B , 24, 107101 (2015).
- M. Takeda, M. Terui, N. Takahashi dan N. Ueda, J. Kimia Keadaan Pepejal , 179, 2823 (2006).
- H. Kuribayashi, S. Makino dan M. Takeda, Abstrak ISBB-18 , 148 (2014).
- M. Terauchi, S. Koshiya dan K. Kimoto, IOP Conf. Siri: Sains Bahan dan Kejuruteraan, 304, 012018 (2017).
- S. Amano, D. Bogdanovski, H. Yamane, M. Terauchi dan R. Dronskowski, Angewandte Chemie , 55, 1652 (2016).
- E. Antonides dan GA Sawatzky, J. Fizik. C: Fizik Keadaan Pepejal ., 9, L547 (1976).
- K. Hirose, M. Kihara, H. Okamoto, S. Shinagawa, H. Nohira, E. Ikenaga, M. Higuchi, A. Teramoto, S. Sugawa, T. Ohmi dan T. Hattori, Surat Fizik Gunaan, 89, 154103 (2006).
- K. Hirose, H. Suzuki, H. Nohira, E. Ikenaga, D. Kobayashi dan T. Hattori, J. Fizik: Siri Persidangan, 100, 01211 (2008).
Adakah anda seorang profesional perubatan atau kakitangan yang terlibat dalam penjagaan perubatan?
Tidak
Sila diingatkan bahawa halaman ini tidak bertujuan untuk memberikan maklumat tentang produk kepada orang ramai.
